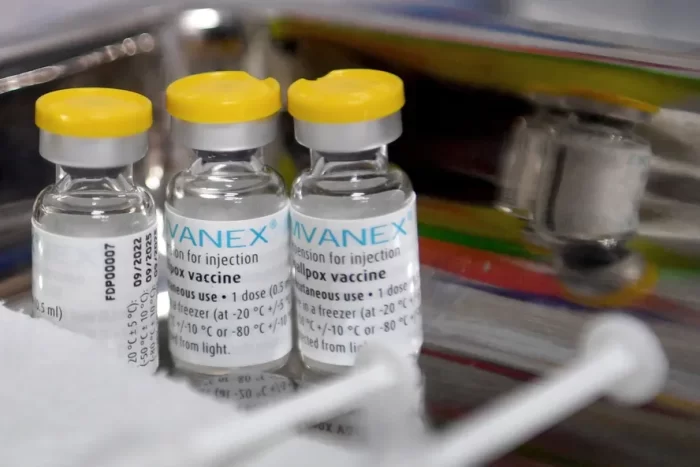Medida tem caráter excepcional e provisório
A diretoria colegiada da Agência Nacional de Vigilância Sanitária (Anvisa) aprovou resolução que dispensa registro e autorização excepcional de importação de medicamentos e vacinas adquiridos pelo Ministério da Saúde para prevenção ou tratamento da mpox.
A medida foi aprovada por unanimidade durante uma reunião da diretoria colegiada. A dispensa de registro será analisada com prioridade pelas áreas técnicas da agência, que deverão tomar uma decisão em até sete dias úteis.
Em caráter provisório e excepcional, a resolução permite ao Ministério da Saúde solicitar à Anvisa a dispensa de registro de medicamentos e vacinas que já tenham sido aprovados por autoridades reguladoras internacionais reconhecidas pela agência para uso contra a mpox.
As autoridades em questão são: Organização Mundial da Saúde (OMS); Agência Europeia de Medicamentos (EMA); Administração de Alimentos e Medicamentos dos Estados Unidos (FDA); Agência Reguladora de Medicamentos e Produtos de Saúde do Reino Unido (MHRA); Agência de Produtos Farmacêuticos e Equipamentos Médicos/Ministério da Saúde, Trabalho e Bem-estar do Japão (PMDA/MHLW); e Agência Reguladora do Canadá (Health Canada).
Segundo a norma, as condições de uso e distribuição dos produtos importados devem seguir exatamente as aprovações das autoridades internacionais. Além disso, todas as fábricas envolvidas na produção, incluindo as linhas de fabricação e formas farmacêuticas, devem ser aprovadas por membros do Esquema de Cooperação em Inspeção Farmacêutica.
A Anvisa espera que seja feito um processo simplificado e prioritário para a importação desses medicamentos e vacinas, semelhante ao modelo utilizado nas importações feitas pela Covax Facility. Neste cenário, o papel do Ministério da Saúde será definir os grupos vulneráveis e prioritários para o uso dos produtos importados. A pasta também terá como responsabilidades monitorar a utilização, acompanhar os pacientes, fornecer orientações para a notificação de eventos adversos e atender a queixas técnicas em colaboração com os serviços de saúde.
Na última semana, a OMS (Organização Mundial da Saúde) declarou pela segunda vez desde 2022 que a mpox é, mais uma vez, uma Emergência de Saúde Pública de Importância Internacional (ESPII). Em seguida, a Anvisa anunciou a criação de um grupo de Emergência em Saúde Pública para gerenciar e monitorar as ações relacionadas à mpox, com duração indeterminada.
A ministra da Saúde, Nísia Trindade, também se manifestou sobre o caso e informou que a pasta a adquiriu 25 mil doses da vacina contra a mpox por meio da Opas (Organização Pan-Americana da Saúde).
Mpox
A mpox, anteriormente conhecida como varíola dos macacos, é uma doença viral causada pelo vírus da família Poxviridae, o mesmo grupo que inclui o vírus da varíola humana. Identificada pela primeira vez em humanos na década de 1970, a mpox é endêmica em algumas regiões da África, especialmente na África Central e Ocidental. O vírus é transmitido principalmente através do contato direto com lesões cutâneas, fluidos corporais ou gotículas respiratórias de indivíduos infectados, além de poder ser transmitido por objetos contaminados.
Em 2022, a Mpox ganhou destaque global ao se espalhar para além das regiões endêmicas, afetando países em todos os continentes, o que levou a Organização Mundial da Saúde (OMS) a declarar uma emergência de saúde pública de importância internacional. Durante esse surto, a doença foi associada a novas vias de transmissão, incluindo o contato sexual, o que facilitou sua disseminação em comunidades antes não afetadas.
A doença geralmente se manifesta com febre, dores musculares, fadiga e erupções cutâneas características que podem evoluir para lesões mais graves. Embora a maioria dos casos seja autolimitada, com sintomas leves a moderados, a Mpox pode ser fatal, especialmente em populações vulneráveis.
(Foto: Francois Lo Presti/AFP)